快讯
医美行业观察

强监管带来“高红利”,合规高质的透明质酸钠企业将迎来增长热潮
导读:随着我国医美行业逐渐成熟,监管力度也逐渐加大。尤其从2021年开始,针对医美产品、机构、营销宣传渠道等各环节实行了全方位整顿,2022 年,医美行业正式迈入合规发展时代。
01 新规之下 透明质酸钠原料的高品质有多重要
5月国家药监局发布公开征求《关于医用透明质酸钠产品管理类别的公告》(修订草案征求意见稿)(下称“意见稿”)进一步将监管细分到医疗器械项目下的透明质酸钠的具体领域。其实早在今年3月30日,国家药品监督管理局对外发布《关于调整《医疗器械分类目录》部分内容的公告(2022年第30号)》(以下简称《目录》)中,已经涉及到对注射用透明质酸钠溶液的监管调整。(详见《医美行业合规新思考|“水光针”产品如何在监管中受益》)

此次《意见稿》是监管升级的具体表现,也对透明质酸钠产品品质提出了更高的要求。总结看来有两个很重要的点:一是医用透明质酸钠产品管理类别不低于第二类;二是注射类透明质酸钠无论是起到塑形还是保湿作用,均按照第三类医疗器械管理。
医用透明质酸钠的监管级别提高,同时在医美领域应用中的监管级别也被明确为三类。监管级别的提高也是对产品品质要求的提升,这也就促使品牌方从原料质量到产品工艺,每一个环节都要做到“极致”。
而原料是一切产品的基础,甚至原料的优劣决定了产品是否合规以及是否有效。在原料端,行业监管上也有一套严格的标准,其中GMP认证是一种适用于制药、食品等行业的强制性标准,据悉,在国内拥有GMP证书的透明质酸钠生产企业只有两家,众山生物便是其中之一。作为一家专注在透明质酸钠原料的企业,多年来不断钻研创新,提升品质。
作为医用透明质酸钠,对细分规格都有严格的标准。众山生物生产的医药级透明质酸钠,在透明质酸钠含量、PH值、无菌性等常规项目上进行了超高的质量把控,除此之外,还严格控制了内毒素、核酸、蛋白、微生物等项目的含量。

以内毒素为例,内毒素是致热源物质,可引起人体发热、热循环障碍、内毒素休克及播散性血管内凝血等。尤其是众山生物的新品系列中的MEDIHYA® I,检测结果<0.005,远低于YY/T 1571规定的0.05。其次核酸含量<0.1,远低于0.5的标准;蛋白质含量<0.05,低于0.1的标准。
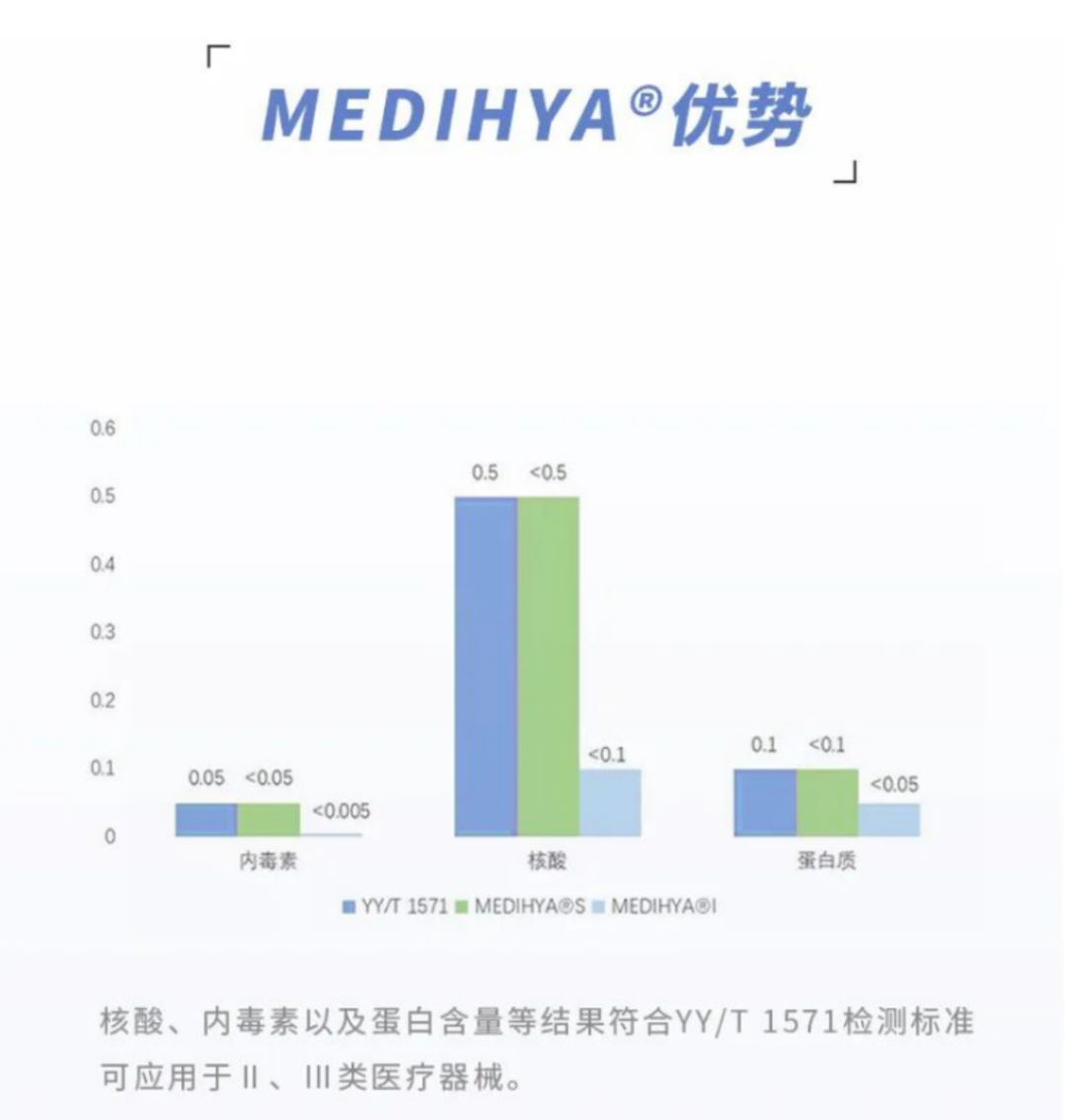
每个环节、品项的标准都在影响最终产品的品质,医美作为“半医半美”的行业更要从源头就开始严格把关,才能用超越标准的优秀品质征服用户。
02 从原料厂家到企业 众山生物靠什么征服市场?
对于原料厂家来说,产品固然是与品牌合作的根基,但随着医美行业地快速爆发,单一的产品生产已经不能满足竞争日益激烈的市场,无论是原料端还是品牌方都需要不断提升。
众山生物在透明质酸钠赛道深耕多年,不断提升,尤其是在监管越来越科学且专业的当下,众山生物在保证产品质量且不断提升的同时,也在不断更新产品线,扩展应用方向等,紧跟市场需求趋势,顺应监管政策。从单纯的透明质酸钠生产厂家逐渐成长为一家有自己特色和优势的原料企业。
众山生物不局限于产品的普通迭代更新,更多的是开拓新的技术、新的产品体验。近期众山生物依据组织工程医疗器械产品透明质酸钠YY/T 1571-2017行业标准,推出了全新的产品系列MEDIHYA® I、MEDIHYA® M和MEDIHYA® S,可应用于Ⅱ、Ⅲ类医疗器械。
除了产品的纵向升级,众山生物在横向扩展产品应用方向上也下了很大功夫。其原料除在润眼液、洗眼液、隐形眼镜护理液等基础的产品中可被广泛应用外,众山生物还针对此次《意见稿》中“作为医用敷料应用时,不被人体吸收或用于非慢性创面医用敷料按二类医疗器械管理”的这一要求,启动了“产品不透皮吸收”的功效实验,力求进一步拓宽产品应用范围,同时也为后续产品合规化审批提供充足的实验数据支持。在不断完善产品矩阵、提高自身的竞争力的同时,也顺应了医美市场产品不断细分化的趋势。
产品优势以外,一家合格优质的原料厂家还应具备优秀的服务能力。透明质酸钠因其特殊性,运输中需冷藏,控制温度以保障产品活性和有效性。所以「温控」运输方案也是考验原料厂家实力的一大要素。根据此前的温控运输记录证明,众山生物的「温控」运输方案是安全且有效的,10天时间里温度几乎保持恒定,最大程度地保障了产品的有效性。
除有效性外,医美产业链条中始终绕不开的一个话题便是安全性。在2021年7月,权威检测机构对众山生物产品进行了细胞毒性、皮肤致敏性、皮内安全性、急性全身毒性等多项生物学测试,检测结果均显示本品在生物体内是具有高度安全性的。

拥有符合行业标准和官方认证“高度安全性”的产品,众山生物获得了权威的肯定,这些资质优势,也能给与众山生物合作的品牌企业带来审批上的便利。众山生物可作为第三方企业在品牌提交审评审批的过程中,提交自己的主文档。
综上,合规、有效、(产品)齐全、安全、稳定,这些“标签”都可以放在众山生物身上,它在原料端的综合实力有目共睹。更重要的是作为原料厂家,众山生物的优势也会更大程度地转嫁到品牌端。
在监管愈发严格、专业的当下,品牌要注重从上到下、从源头到终端产品的把关,才有可能达到事半功倍的效果。
医美行业处于大爆发阶段,透明质酸钠作为行业中起中流砥柱作用的领域不仅备受关注,而且发展潜力巨大。在监管不断加强的情况下,透明质酸钠将是首个被完善的领域,也促使其产业链上下游进入新一轮良性竞争。
唯有始终坚持高品质,不断突破创新的企业才能走得更远。而对于品牌方来说,要做长期主义,选择对的合作伙伴至关重要,尤其是作为源头的原料厂家,是一切后续程序的根基。再加上监管带来合规红利,优秀、有实力的企业必将脱颖而出。
文章来源:医美产业笔记
版权声明:转载医美医美行业观察的原创文章,需注明文章来源以及作者名称。公众号转载请联系开白小助手(微信号:pingshalaile)。违规转载法律必究。

扫描二维码,第一时间获取医美行业的资讯和动态。
从此和医美医美行业观察建立直接联系。
本栏目文字内容归ymguancha.com所有,任何单位及个人未经许可,不得擅自转载使用。
Copyright © 医美行业观察 | 京ICP备20027311号-1
参与评论